Butan Tokeletes Egese
A Bután Tökéletes Égése: Átfogó Útmutató
Ebben a részletes cikkben mélyrehatóan megvizsgáljuk a bután tökéletes égésének folyamatát. Célunk, hogy mindenre kiterjedő ismereteket nyújtsunk a kémiai reakció mechanizmusától kezdve a gyakorlati alkalmazásokig. Megértjük a reakció egyenletét, a keletkező termékeket, az energiafelszabadulást és azt, hogy miért nevezzük ezt “tökéletes” égésnek. Emellett kitérünk a biztonsági szempontokra és a bután felhasználásának különböző területeire.
Mi a Bután? Alapvető Kémiai Tulajdonságok
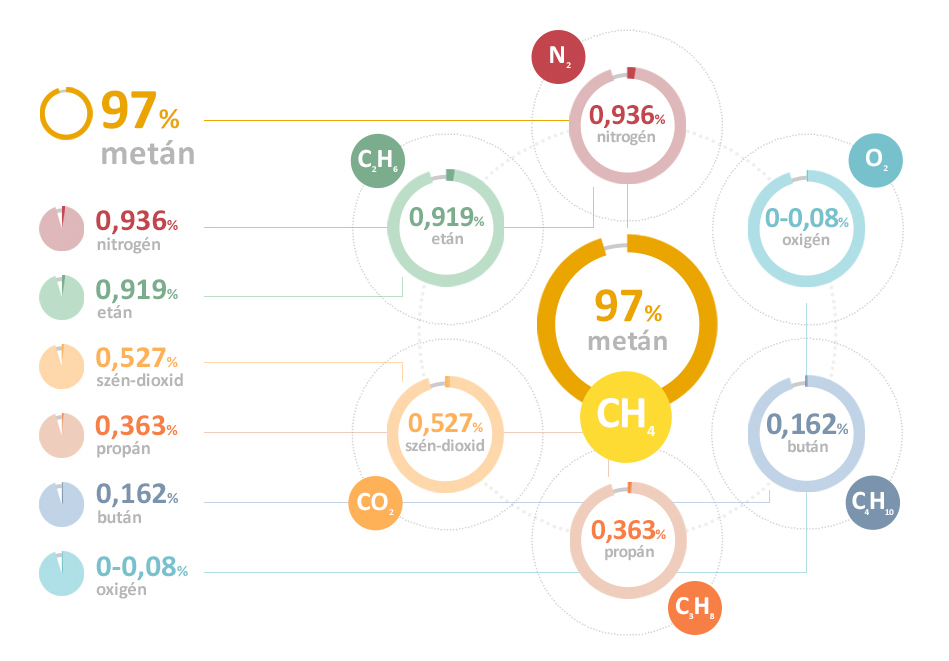
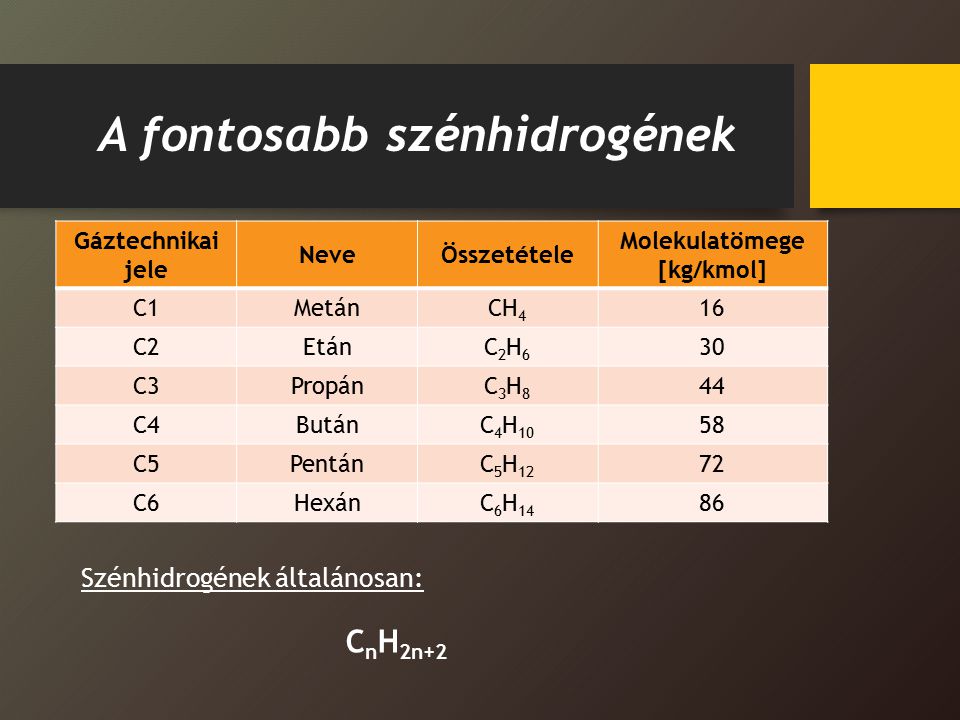
A bután egy négy szénatomos alkán, amelynek kémiai képlete $\mathbf{C_4H_{10}}$. Szobahőmérsékleten és légköri nyomáson színtelen, szagtalan gáz. A bután a földgáz és a kőolaj feldolgozásának melléktermékeként keletkezik. Kiváló tüzelőanyag, magas fűtőértékkel rendelkezik, ezért széles körben használják háztartásokban és ipari alkalmazásokban egyaránt. Két izomerje létezik: az n-bután (egyenes láncú) és az izobután (elágazó láncú). A mindennapi életben gyakran propánnal keverve, propán-bután gáz formájában találkozhatunk vele, amelyet például gázpalackokban tárolnak.
A Bután Fizikai Tulajdonságai
A bután forráspontja körülbelül -0.5 °C, ami azt jelenti, hogy normál körülmények között gáz halmazállapotú. Sűrűsége a levegőnél nagyobb, ezért szivárgás esetén a föld közelében terjed. Vízben rosszul oldódik, de sok szerves oldószerrel elegyedik. Gyúlékony gáz, levegővel keveredve robbanásveszélyes lehet egy bizonyos koncentrációtartományban (az alsó és felső robbanási határ között).
A Bután Kémiai Tulajdonságai
A bután telített szénhidrogén, ami azt jelenti, hogy szénatomjai között csak egyszeres kötések találhatók. Ez viszonylag stabil molekulává teszi. Legjellemzőbb kémiai reakciója az égés, amely során oxigénnel reagálva hő és fény szabadul fel. A tökéletes égés során a szén-dioxid ($\mathbf{CO_2}$) és a víz ($\mathbf{H_2O}$) keletkezik.
A Tökéletes Égés Fogalma és Jelentősége
A tökéletes égés egy olyan kémiai folyamat, amely során egy üzemanyag (jelen esetben a bután) elegendő mennyiségű oxigénnel reagál, és a reakciótermékek a lehető legoxidáltabb formában jelennek meg. Szénhidrogének, mint a bután, tökéletes égésekor szén-dioxid és víz keletkezik. Fontos megjegyezni, hogy a tökéletes égés ideális körülmények között következik be, ahol a levegő és az üzemanyag tökéletesen keveredik, és elegendő oxigén áll rendelkezésre a teljes reakcióhoz.
A Tökéletlen Égés Esete
Ezzel szemben a tökéletlen égés akkor következik be, ha nem áll rendelkezésre elegendő oxigén, vagy a keveredés nem megfelelő. Ilyenkor a szén-dioxid és a víz mellett más termékek is keletkezhetnek, mint például szén-monoxid ($\mathbf{CO}$), korom (elemi szén, $\mathbf{C}$) és egyéb részlegesen oxidált szénhidrogének. A szén-monoxid egy mérgező gáz, a korom pedig lerakódásokat okozhat a berendezésekben és a levegő minőségét is rontja.
A Bután Tökéletes Égésének Kémiai Egyenlete
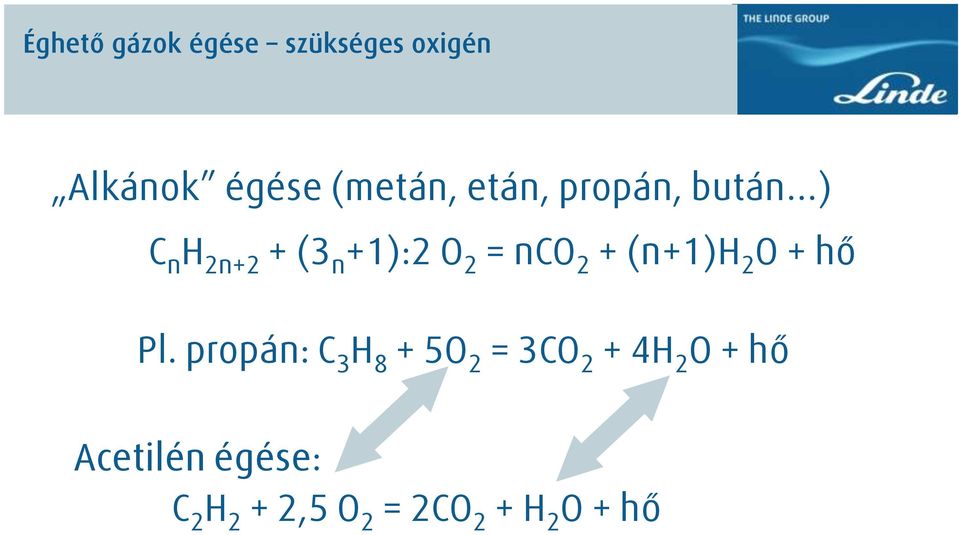
A bután tökéletes égésének kiegyenlített kémiai egyenlete a következő:
$$\mathbf{2 C_4H_{10} + 13 O_2 \rightarrow 8 CO_2 + 10 H_2O}$$
Ez az egyenlet azt mutatja, hogy két molekula bután tizenhárom molekula oxigénnel reagálva nyolc molekula szén-dioxidot és tíz molekula vizet hoz létre. A reakció során jelentős mennyiségű energia, főként hő formájában szabadul fel.
A Reakció Lépései Molekuláris Szinten
Molekuláris szinten a bután égése egy komplex folyamat, amely több elemi lépésből áll. Először a bután és az oxigén molekulák ütköznek. Ha az ütközés energiája elegendő a kémiai kötések felbontásához, akkor a reakció megindul. A szénhidrogén-láncban lévő C-H és C-C kötések felbomlanak, és új kötések alakulnak ki a szénatomok és az oxigén, valamint a hidrogénatomok és az oxigén között, létrehozva a szén-dioxidot és a vizet. Ez a folyamat láncreakcióként is felfogható, ahol a kezdeti reakciók további reaktív intermedier termékeket hoznak létre, amelyek aztán tovább reagálnak.
Az Égéshez Szükséges Feltételek
Ahhoz, hogy a bután égése bekövetkezzen, három alapvető feltételnek kell teljesülnie, amelyet gyakran az “égési háromszög” szemléltet:
- Üzemanyag: Jelen esetben a bután gáz.
- Oxidálószer: Általában a levegőben található oxigén ($\mathbf{O_2}$).
- Gyújtóforrás: Olyan energiaforrás, amely elegendő energiát biztosít a reakció beindításához (pl. szikra, láng, forró felület).
Ha ezen feltételek bármelyike hiányzik, az égés nem indul meg vagy nem marad fenn.
A Levegő Szerepe az Égésben
A legtöbb gyakorlati alkalmazásban az oxigént a levegő biztosítja, amely körülbelül 21% oxigént tartalmaz. A levegőben található többi gáz, főként a nitrogén, nem vesz részt közvetlenül az égési reakcióban, de befolyásolhatja a folyamatot (pl. hűtő hatásával).
A Tökéletes Égés Termékei: Szén-dioxid és Víz
Amint azt a kémiai egyenlet is mutatja, a bután tökéletes égésének két fő terméke a szén-dioxid ($\mathbf{CO_2}$) és a víz ($\mathbf{H_2O}$).
Szén-dioxid ($\mathbf{CO_2}$)
A szén-dioxid egy színtelen, szagtalan gáz, amely a légkörünk természetes alkotóeleme. Azonban a fosszilis tüzelőanyagok (mint a bután) égetése hozzájárul a légköri szén-dioxid koncentrációjának növekedéséhez, ami hatással van a globális klímára. A tökéletes égés során keletkező szén-dioxid azt jelzi, hogy a szénatomok a lehető legmagasabb oxidációs állapotba kerültek.
Víz ($\mathbf{H_2O}$)
A víz a hidrogén és az oxigén vegyülete. A bután égésekor víz gőz formájában keletkezik, amely lehűlés hatására kondenzálódhat. A tökéletes égés során keletkező víz azt jelzi, hogy a hidrogénatomok is a lehető legmagasabb oxidációs állapotba kerültek.
Az Energia Felszabadulása a Bután Égésekor
A bután égése exoterm reakció, ami azt jelenti, hogy hő szabadul fel a folyamat során. A felszabaduló hő mennyisége függ az elégetett bután mennyiségétől. A bután magas fűtőértékkel rendelkezik, ezért hatékony tüzelőanyag. A felszabaduló energia felhasználható fűtésre, főzésre, vagy akár elektromos áram előállítására is.
A Fűtőérték Fogalma
A fűtőérték megadja, hogy egy egységnyi mennyiségű üzemanyag (tömeg vagy térfogat) elégetésekor mennyi hőenergia szabadul fel. A butánnak magas az alsó és a felső fűtőértéke is, ami ideálissá teszi számos energetikai alkalmazáshoz.
A Bután Felhasználási Területei
A bután széles körben elterjedt tüzelőanyag a különböző területeken:
Háztartási Használat
A háztartásokban a butánt gyakran használják gáztűzhelyekhez, sütőkhöz és hordozható gázfűtő berendezésekhez. A propán-bután keveréket tartalmazó gázpalackok népszerűek kempingezéshez és olyan helyeken, ahol nincs kiépített gázhálózat.
Ipari Alkalmazások
Az iparban a butánt fűtési célokra, valamint egyes kémiai folyamatokban reagensként is alkalmazzák. Például a petrolkémiai iparban a butánt más vegyületek előállítására használják.
Autógáz (LPG)
A propánnal kevert butánt autógázként (LPG – Liquefied Petroleum Gas) is használják, amely egy alternatív üzemanyag a benzin és a dízel mellett.
Aeroszolok
A butánt és izobutánt hajtógázként is alkalmazzák aeroszolos termékekben, például dezodorokban és hajlakkokban.
Biztonsági Szempontok a Bután Használatakor

Bár a bután sokoldalú és hasznos energiaforrás, a használata során bizonyos biztonsági előírásokat be kell tartani:

Gyúlékonyság és Robbanásveszély
A bután gyúlékony gáz, és levegővel keveredve robbanásveszélyes lehet. Ezért fontos a szellőztetés olyan helyeken, ahol butánt használnak vagy tárolnak, és kerülni kell a nyílt lángot és a szikraképződést.
Szivárgás Érzékelése
Mivel a tiszta bután szagtalan, gyakran szagosító anyagokat adnak hozzá, hogy a szivárgás könnyen észlelhető legyen. Gázszivárgás esetén azonnal el kell zárni a gázt, szellőztetni kell a helyiséget, és értesíteni kell a szakembereket.
Helyes Tárolás
A butánt tartalmazó palackokat megfelelően szellőző helyen, távol hőforrástól és gyújtóforrástól kell tárolni. A sérült palackokat nem szabad használni.
Összefoglalás: A Bután Tökéletes Égésének Fontossága
A bután tökéletes égése egy alapvető kémiai folyamat, amelynek megértése elengedhetetlen a különböző energetikai és ipari alkalmazások szempontjából. A reakció során szén-dioxid és víz keletkezik, miközben jelentős mennyiségű hőenergia szabadul fel. A biztonságos és hatékony felhasználás érdekében fontos a tökéletes égés feltételeinek biztosítása és a biztonsági előírások betartása.

További Tudnivalók és Kapcsolódó Témák
- A tökéletlen égés káros hatásai.
- A különböző szénhidrogének égése.
- A fűtőérték számítása.
- A bután környezeti hatásai.
Reméljük, hogy ez az átfogó cikk minden szükséges információt tartalmazott a bután tökéletes égésével kapcsolatban. Ha további kérdése van, ne habozzon felvenni velünk a kapcsolatot!