Kovalens Kotes Felszakitasa
A Kovalens Kötés Felszakítása: Átfogó Tanulmány
A kovalens kötés felszakítása a kémiai reakciók alapvető lépése, amely meghatározza a termékek képződésének útját és a reakció sebességét. Ebben a részletes tanulmányban mélyrehatóan vizsgáljuk a kovalens kötések felbomlásának mechanizmusait, a folyamatot befolyásoló tényezőket, valamint a különböző alkalmazási területeket. Célunk, hogy átfogó képet nyújtsunk erről a központi kémiai jelenségről.
A Kovalens Kötés Természete és Erőssége
Mielőtt a kötésfelszakítás részleteibe merülnénk, elengedhetetlen megérteni a kovalens kötés alapvető természetét. A kovalens kötés akkor jön létre, amikor két atom megosztja elektronjait, hogy stabilisabb elektronkonfigurációt érjen el, jellemzően a nemesgáz konfigurációját. A megosztott elektronpárok vonzzák mindkét atom magját, létrehozva ezzel a kötést. A kovalens kötések erőssége változó lehet, függően a kötött atomok típusától, a kötés többszörösségétől (szimpla, dupla, tripla), valamint a molekula általános szerkezetétől.
A Kötési Energia Szerepe
A kötési energia az a minimális energia, amely szükséges egy molnyi gázfázisú molekulában egy adott kovalens kötés felszakításához homolitikusan, azaz úgy, hogy mindkét atom egy-egy elektront visz el a kötőelektronpárból. A magasabb kötési energia erősebb kötést jelent, amelynek felszakításához több energia szükséges. A kötési energia értékei táblázatokban megtalálhatók, és kulcsfontosságúak a reakciók entrópiájának és entalpiájának, valamint a reakcióképesség megértéséhez.
A Kötéshossz Hatása
A kötéshossz, a két kötött atom magjainak távolsága, szintén befolyásolja a kötés erősségét. Általánosságban elmondható, hogy rövidebb kötések erősebbek, mivel az atommagok és a megosztott elektronok közötti vonzóerő nagyobb. A kötéshossz függ az atomok méretétől és a kötés többszörösségétől.
A Kovalens Kötés Felszakításának Mechanizmusai

A kovalens kötések két fő mechanizmus szerint szakadhatnak fel: homolízis és heterolízis.
Homolízis: Szimmetrikus Kötésfelszakítás
A homolízis során a kovalens kötést alkotó elektronpár egyenlően oszlik meg a két atom között. Mindkét atom egy-egy elektront kap a kötésből, ami szabad gyökök képződéséhez vezet. A szabad gyökök párosítatlan elektronnal rendelkező, rendkívül reaktív kémiai specieszek. A homolízis gyakran magas hőmérsékleten vagy sugárzás hatására következik be, mivel energiát kell befektetni a szimmetrikus kötésfelszakításhoz.
A Szabad Gyökök Képződése és Reaktivitása
A szabad gyökök rendkívül reaktívak, mivel elektronhiányosak. Hajlamosak elektronokat felvenni más molekuláktól, ami láncreakciókhoz vezethet. A szabad gyökök reakciói fontos szerepet játszanak számos folyamatban, beleértve a polimerizációt, az égést és a biológiai rendszerek oxidatív károsodását.
Heterolízis: Aszimmetrikus Kötésfelszakítás
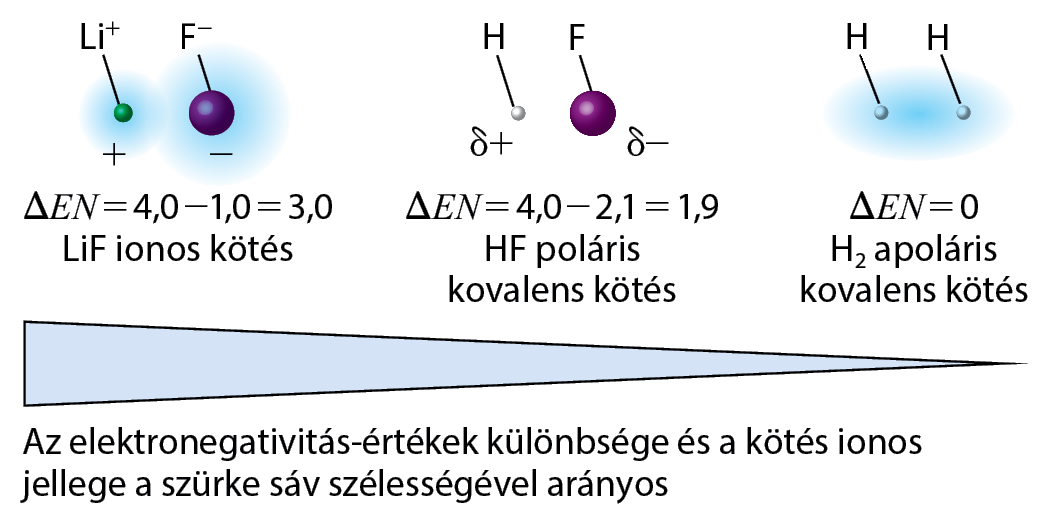
A heterolízis során a kovalens kötést alkotó elektronpár mindkét elektronja az egyik atomnál marad, míg a másik atom elektronhiányossá válik. Ez ionok képződéséhez vezet: egy pozitív töltésű kationhoz és egy negatív töltésű anionhoz. A heterolízis gyakrabban fordul elő poláris kovalens kötések esetén, ahol az egyik atom elektronegatívabb, mint a másik.
A Kationok és Anionok Képződése és Stabilitása

A kationok és anionok stabilitását számos tényező befolyásolja, beleértve az atomok elektronegativitását, a molekula szerkezetét és a környező oldószer polaritását. Poláris oldószerek, például a víz, stabilizálhatják az ionokat szolvatációval, ami elősegítheti a heterolitikus kötésfelszakítást.
A Kötés Felszakítását Befolyásoló Tényezők
Számos tényező befolyásolja a kovalens kötés felszakításának valószínűségét és módját.
Hőmérséklet Hatása
A hőmérséklet növelése általában növeli a molekulák kinetikus energiáját, ami megkönnyíti a kötések rezgését és nyúlását, ezáltal elősegítve a felszakadásukat. Magasabb hőmérsékleten a homolízis valószínűsége nő.
Sugárzás Hatása
A sugárzás, különösen az ultraibolya (UV) fény és a nagy energiájú sugárzás, elegendő energiát szolgáltathat a kovalens kötések felszakításához. A fotokémiai reakciók gyakran sugárzás hatására indulnak el homolitikus kötésfelszakadással.
Oldószer Hatása
Az oldószer polaritása jelentősen befolyásolhatja a kötésfelszakítás mechanizmusát. Poláris oldószerek elősegítik a heterolízist azáltal, hogy stabilizálják a keletkező ionokat, míg apoláris oldószerek a homolízist részesíthetik előnyben.
Katalizátorok Szerepe
A katalizátorok olyan anyagok, amelyek megnövelik a reakció sebességét anélkül, hogy maguk elfogynának a reakció során. A katalizátorok gyakran úgy működnek, hogy alternatív reakcióutat kínálnak alacsonyabb aktiválási energiával, ami megkönnyítheti a kovalens kötések felszakítását.
A Kovalens Kötés Felszakításának Fontossága a Kémiában
A kovalens kötés felszakítása központi szerepet játszik a kémia számos területén.
Szerves Kémiai Reakciók
A szerves kémiai reakciók többsége magában foglalja meglévő kovalens kötések felszakítását és új kötések kialakulását. A reakciómechanizmusok részletes megértése elengedhetetlen a termékek előrejelzéséhez és a reakciók optimalizálásához.
SN1 és SN2 Reakciók
Az SN1 (unimolekuláris nukleofil szubsztitúció) és SN2 (bimolekuláris nukleofil szubsztitúció) reakciók klasszikus példák a heterolitikus kötésfelszakításra a szerves kémiában. Az SN1 reakciókban az első lépés a távozó csoport heterolitikus leválása, ami egy karbokation intermediert eredményez. Az SN2 reakciókban a nukleofil támadás és a távozó csoport leválása egyetlen összehangolt lépésben történik.
Gyökös Reakciók
A gyökös reakciók homolitikus kötésfelszakítással indulnak, ami szabad gyökök képződéséhez vezet. Ezek a gyökök aztán láncreakciókon keresztül reagálhatnak más molekulákkal.
Polimerizáció
A polimerizáció során kis monomerek kapcsolódnak össze hosszú láncú polimerekké. A láncreakciós polimerizációk gyakran gyökös mechanizmuson keresztül mennek végbe, amelynek iniciálása egy kovalens kötés homolitikus felszakítását igényli az iniciátorban.

Katalízis
A katalitikus ciklusok számos lépést foglalnak magukban, amelyek közül néhány kovalens kötések felszakítását és kialakítását tartalmazza. A katalizátorok megkönnyítik ezeket a lépéseket azáltal, hogy alacsonyabb energiájú reakcióutakat biztosítanak.

A Kovalens Kötés Felszakításának Vizsgálati Módszerei
Számos kísérleti és elméleti módszer áll rendelkezésünkre a kovalens kötések felszakításának tanulmányozására.
Kinetikai Vizsgálatok
A kinetikai vizsgálatok a reakciósebesség mérésén alapulnak, ami információt nyújt a reakció mechanizmusáról, beleértve a kötésfelszakítás lépését is. A sebességi állandók és a reakció rendje meghatározható kísérleti adatokból.
Spektroszkópiai Módszerek
A spektroszkópiai módszerek, mint például az infravörös (IR) spektroszkópia és a magmágneses rezonancia (NMR) spektroszkópia, információt nyújtanak a molekulák szerkezetéről és a kémiai kötések állapotáról, ami segíthet a kötésfelszakítás folyamatának megértésében.
Tömegspektrometria
A tömegspektrometria a molekulák és fragmentjeik tömeg-töltés arányának mérésén alapul. A fragmentációs mintázatok információt nyújthatnak a molekulában lévő gyenge kötések helyéről, amelyek könnyebben szakadnak fel.
Kvantumkémiai Számítások
A kvantumkémiai számítások lehetővé teszik a molekulák elektronikus szerkezetének és energiájának modellezését. Ezek a számítások segíthetnek a kötési energiák, a reakcióutak és az átmeneti állapotok megjóslásában, ezáltal mélyebb betekintést nyújtva a kötésfelszakítás folyamatába.
Gyakorlati Alkalmazások
A kovalens kötés felszakításának megértése számos technológiai és ipari alkalmazás szempontjából kritikus fontosságú.
Anyagtudomány
Az anyagtudományban a polimerek előállítása és a különböző anyagok lebomlása (például a műanyagok degradációja) kovalens kötések felszakítását foglalja magában. A kötésfelszakítás mechanizmusának ismerete lehetővé teszi új anyagok tervezését és a meglévők tulajdonságainak javítását.
Gyógyszeripar
A gyógyszeriparban a gyógyszermolekulák hatásmechanizmusának megértéséhez elengedhetetlen a kémiai kötések, beleértve a kovalens kötéseket is, kialakulásának és felszakadásának ismerete a biológiai célpontokkal. Bizonyos gyógyszerek kovalens kötéssel kötődnek a célfehérjékhez, ami irreverzibilis gátlást eredményez.
Környezetvédelem
A környezetvédelemben a szennyező anyagok lebontásának folyamatai gyakran kovalens kötések felszakítását foglalják magukban. A fotokatalitikus lebontás, például, fény segítségével aktiválja a katalizátorokat, amelyek aztán a szennyező molekulákban lévő kovalens kötéseket hasítják fel.
Összefoglalás
A kovalens kötés felszakítása egy alapvető kémiai folyamat, amely számos kémiai reakció és technológiai alkalmazás szempontjából kulcsfontosságú. A homolízis és a heterolízis két fő mechanizmus, amelyek eltérő termékekhez (szabad gyökökhöz, illetve ionokhoz) vezetnek. A kötésfelszakítást számos tényező befolyásolja, beleértve a hőmérsékletet, a sugárzást, az oldószert és a katalizátorokat. A folyamat megértése elengedhetetlen a szerves kémia, a polimerizáció, a katalízis, az anyagtudomány, a gyógyszeripar és a környezetvédelem területén. A kovalens kötések felszakításának vizsgálatára számos kísérleti és elméleti módszer áll rendelkezésünkre, amelyek együttesen átfogó képet nyújtanak erről a komplex jelenségről.
További Kutatási Irányok
A kovalens kötés felszakításával kapcsolatos kutatások területe folyamatosan fejlődik. Jelenleg nagy hangsúlyt fektetnek a szelektivitás növelésére a kötésfelszakítási reakciókban, valamint az új katalitikus rendszerek kifejlesztésére, amelyek képesek alacsonyabb energiaigénnyel végrehajtani ezeket a folyamatokat. A számítógépes kémia fejlődése lehetővé teszi a reakciómechanizmusok részletesebb feltárását és a reakciók előrejelzését.
Kihívások és Lehetőségek
Az egyik legnagyobb kihívás a kovalens kötések szelektív felszakítása komplex molekulákban. A különböző típusú kötések jelenléte egy molekulán belül megnehezíti egy adott kötés célzott hasítását. Azonban az új katalitikus módszerek és a precíziós kémia eszközei ígéretes lehetőségeket kínálnak ezen a területen.
Következtetés
A kovalens kötés felszakításának alapos ismerete elengedhetetlen a modern kémia és a kapcsolódó tudományterületek számára. A folyamat mechanizmusainak, a befolyásoló tényezőknek és a gyakorlati alkalmazásoknak a megértése lehetővé teszi új technológiák fejlesztését és a meglévő folyamatok optimalizálását. Reméljük, hogy ez az átfogó tanulmány hozzájárult a kovalens kötés felszakításával kapcsolatos ismeretek bővítéséhez.